2024年8月30日、厚労省が来年度(2025年度、令和7年度)の予算要求の概要を公表しました。(令和7年度厚生労働省所管予算概算要求関係)
この予算要求概要の内容は、財務省と折衝済みのものとなりますので、2025年4月からの厚労省の施策については、この予算要求の概要に基づいて実施されていくことになります。
今回の要求では、ドラッグ・ロス対策等、骨太方針2024や創薬エコシステムサミット(2024年7月30日開催)の内容を踏まえたものとなっています。また、厚生労働省国際保健ビジョン(2024年8月26日公表)の内容も入れこんできていました。
以下、厚労省の概算要求のうち、医薬品、医療機器、再生医療等製品に関するめぼしい施策を確認しておきます。
2025年度予算概算要求の概要
こちらに概算要求の概要が掲載されています。

特筆すべきは、創薬力強化のトピックが一番最初にきていることです。先の創薬サミットを含め、厚労省、政府として引き続き優先的に取り組む必要性を感じていることの表れです。
上記青枠にある「全世代型社会保障の実現に向けた保健・医療・介護の構築」に関連して、医薬品、医療機器、再生医療等製品に関連した施策の予算が要求されています。
2025年度予算概算要求のうち、医薬品、医療機器、再生医療等製品に関するめぼしい施策
主要施策は、こちらの掲載されています。そこから、めぼしい施策を以下に挙げていきます。
新規モダリティ対応ヒト初回投与試験体制整備等事業

骨太方針、構想力会議を踏まえた創薬力サミットでも強く発信されていた、ファースト・イン・ヒューマン(FIH)試験実施体制整備が最初にきています。
この体制整備予算は、(公募ではなく)決め打ちで国立施設に手当することになっています。国立がん研究センター、国立健康危機管理研究機構(旧:国立国際医療研究センター)及び国立成育医療研究センターが対象とされています。
国立がん研究センターのみ、FIH試験の体制整備に加えて、医薬品の製造機能と研究を併設した体制の整備となっています。
国立がんセンターで製造設備を併設させてどのような薬剤を製造しようとしているのか、国立成育医療研究センターでFIH試験の体制強化でどのような試験をしようとしているのか、狙いどころがイマイチ明確ではない部分はありますが、とりあえず、宣言通り体制は整備していくことになりそうです。
国際共同治験ワンストップ相談窓口事業
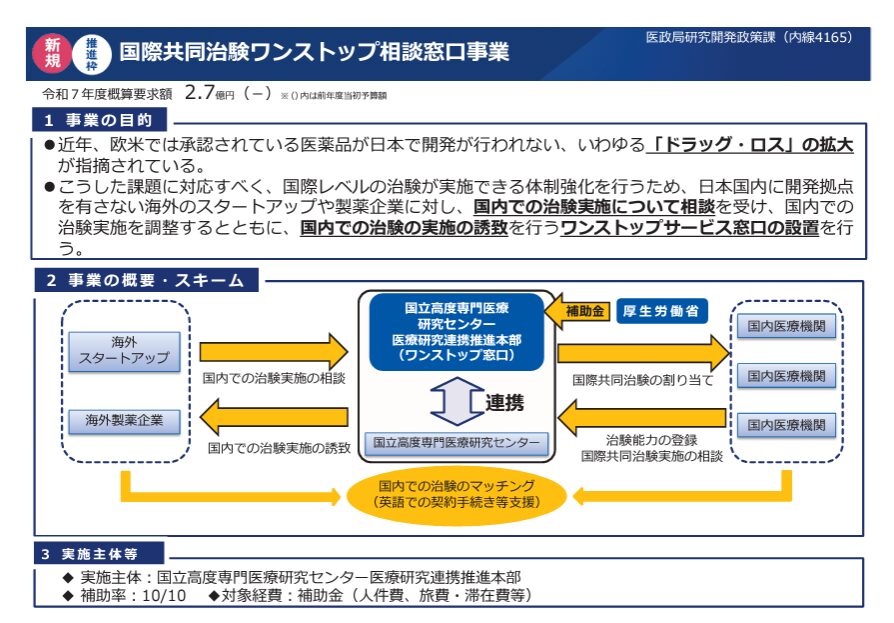
こちらも決め打ち予算で、国立高度専門医療研究センター医療研究連携推進本部が対象となっています。国立高度専門医療研究センター医療研究連携推進本部は、上記、国立がんセンターや国立成育医療センター等国立センターの調整機能的な組織になります。
この相談窓口業務も、骨太方針や構想力会議でも常々提唱されていたものがそのまま施策となっています。この枠でカバーできる治験(と被験者数)がどの程度となるのかが気になるところです。組織維持のための人件費で終わらないことを期待です。
創薬基盤強化支援事業
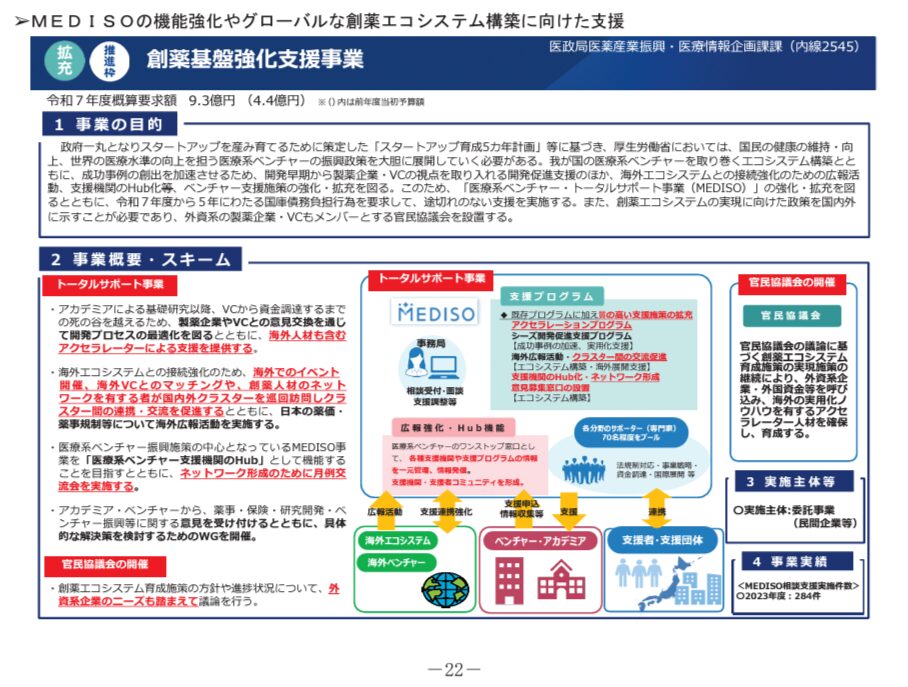
構想力会議の目玉であった官民協議会及びそれに関連した創薬エコシステムの構築を目的とした予算になっています。5億円近く(既存施策の倍額まで)の増額が何に使われるのかよく分かりませんが、サポーター(専門家)の人件費が想定されているのかもしれません。
小児医薬品開発支援体制強化事業

国立成育医療センターへの補助になります。小児医薬品開発促進を主導できるよう、予算面からのサポートとなっています。
PMDA小児・希少疾病用医薬品等薬事相談センター事業

資料にもありますが、すでに2024年7月から実施している相談手数料等の補助について、2025年度も継続するための予算要求となります。
2000万円のみの増額ですが、未承認薬検討会の新スキーム対応(国の主導的な未承認薬の特定、評価)や希少疾病用医薬品の指定増加への対応のための審査人員が追加対応として想定されています。希少疾病用医薬品については、PMDAの体制の問題で、指定されたにも関わらず、優先対応の対象となっていない品目が発生しています。関連する通知は2024年1月に発出されており、「1年後を目処に、・・・、見直しを検討」とされていますので、この予算での手当を含めて、適切な対応へと見直しがされるのかは注視が必要です。
創薬力強化のための早期薬事相談・支援事業
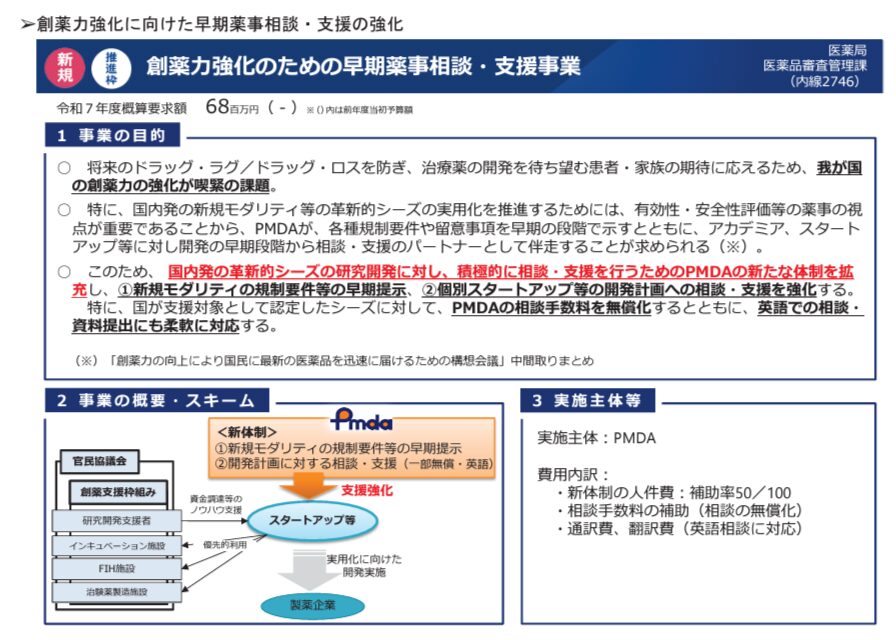
PMDAの相談体制強化の予算になります。官民協議会が絡んだ話にもなっていますが、国が支援対象と認定したシーズ(国内発とは言っていない)に関して、PMDA相談手数料の無料化、英語での相談、資料提出を認めるということにも言及されています。
翻訳費用を用意するということですが、これまで申請者(相談者)側で要していた翻訳の費用、時間をPMDA側でカバーするという見方もできます。相談の申し込みから実施までに実質3か月間であって、PMDAの持ち時間はより短い中、どこまで翻訳で対応しきれるのかは気になるところです。
リアルワールドデータの活用等によるプログラム医療機器実用化促進事業
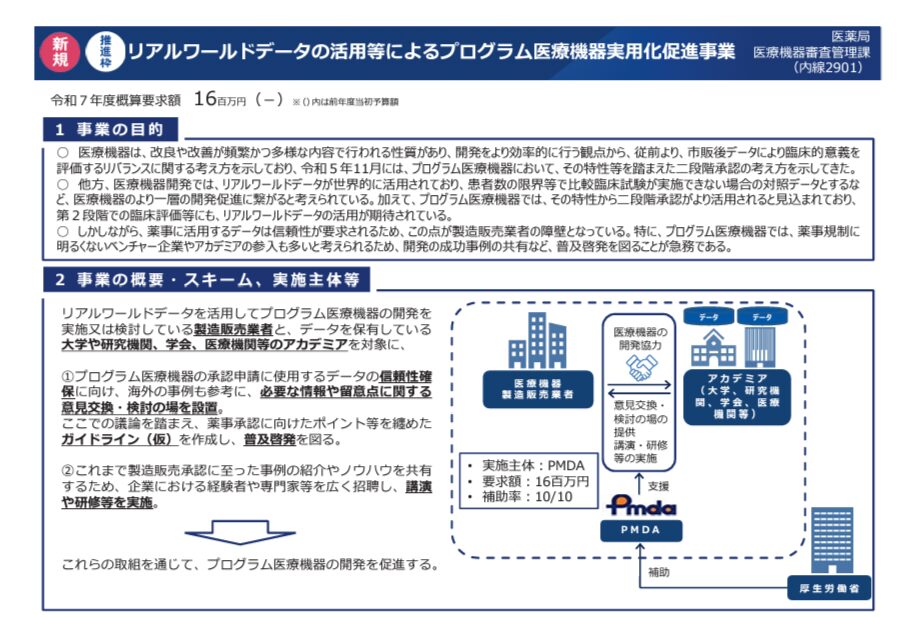
プログラム医療機器(SaMD)への対応は、引き続き、注力されており、関連する予算要求がいくつかります。その中で、本施策は新規の予算要求事項になります。SaMDに活用するデータの信頼性確保に向けて、ガイドラインの作成と普及活動をするための予算となっています。
優れた医療機器の創出に係る産業振興拠点強化事業
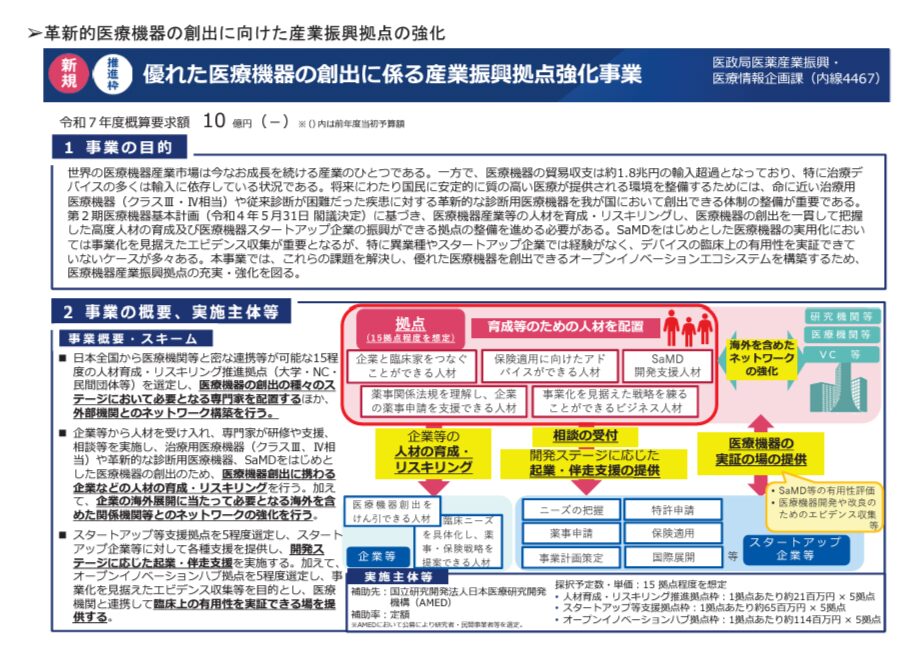
医薬品のエコシステム、官民協議会ではないですが、医療機器でも関係者が集まる会議体を作って、いろいろとやりましょう、というための予算となっています。
臨床研究・治験推進研究事業

AMED予算に関連したもので、既存予算の拡充になります。治験の体制整備のうち、アジア地域での治験実施体制の整備になります。資料中にハイライトされていますが、国境を越えた分散型臨床試験(DCT)の体制整備、感染症緊急事態に対応した体制整備、現地拠点の更なる強化といったことに主眼が置かれています。
医薬品安定供給・流通確認システム(仮称)の開発

メールベースで収集している「供給状況報告」と「供給不安報告」を情報システムに入力できるようにするための予算です。もっと早くできなかったの?という施策です。
GMP管理体制強化等事業

2024年4月からの医薬品医療機器制度部会から次期薬機法改正の議論が開始されていますが、その中で、GMP調査主体を基本的に都道府県からPMDAに見直すという議論が出ています。しかしながら、2025年度予算では引き続き、都道府県のGMP調査能力の向上のための予算も要求しています。
UHCナレッジハブ

無事(?)、予算要求事項となっています。
認知症政策研究事業

新規予算要求となりますが、認知症の早期発見・介入に向けて、自治体経由で大規模な実証プロジェクトを実施するとのこと。このような研究の成果が日の目をみることを期待しています。
関連リンク
- 令和7年度厚生労働省所管予算概算要求関係:https://www.mhlw.go.jp/wp/yosan/yosan/25syokan/index.html
- 令和7年度厚生労働省予算概算要求の概要:https://www.mhlw.go.jp/wp/yosan/yosan/25syokan/dl/01-01.pdf
- 経済財政運営と改革の基本方針2024 内閣府ホームページ:https://www5.cao.go.jp/keizai-shimon/kaigi/cabinet/honebuto/2024/decision0621.html
- 経済財政運営と改革の基本方針2024(骨太方針2024) 本文:https://www5.cao.go.jp/keizai-shimon/kaigi/cabinet/honebuto/2024/2024_basicpolicies_ja.pdf
- 創薬力の向上により国民に最新の医薬品を迅速に届けるための構想会議のホームページ:https://www.cas.go.jp/jp/seisaku/souyakuryoku/index.html
- 中間とりまとめの概要:https://www.cas.go.jp/jp/seisaku/souyakuryoku/pdf/chuukantorimatome_gaiyou.pdf
- 中間とりまとめ:https://www.cas.go.jp/jp/seisaku/souyakuryoku/pdf/chuukantorimatome.pdf
中間とりまとめを踏まえた政策目標と工程表:https://www.cas.go.jp/jp/seisaku/souyakuryoku/pdf/chuukantorimatome_mokuhyou.pdf - 中間とりまとめ:創薬力の向上により国民に最新の医薬品を迅速に届けるための構想会議(2024年5月22日):https://regulatory-j.com/2024-proposal/
- 「厚生労働省国際保健ビジョン」の公表について:https://www.mhlw.go.jp/stf/newpage_42939.html


コメント