2025年2月13日付けで「年次報告に係る変更手続導入に向けた試行的実施について」(医薬品審査管理課長通知)が発出されました。
薬機法の制度上、医薬品の製造方法等の変更にあたっては、承認事項の一部変更に係る申請(一変申請)と軽微な変更に係る届出(軽微変更届)の手続きがあります。
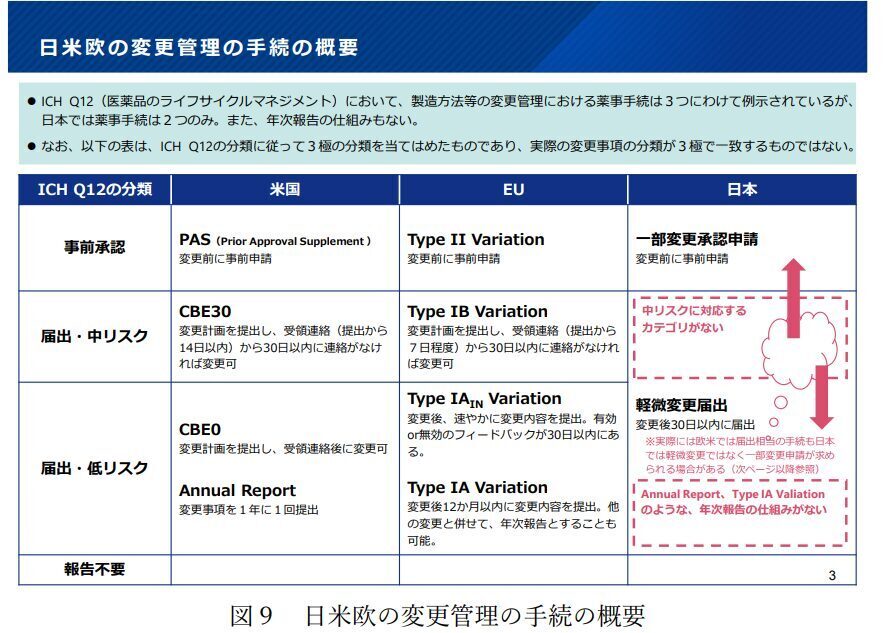
「創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会」の報告書でも言及がありましたが、欧米の制度と比較した場合に中リスクの変更に関して、迅速に処理されない点が指摘されていました。(関連記事)
上記指摘のうち、2024年9月27日からは中等度変更事項に係る変更手続の試行導入が実施されています。(関連記事)
今回は、製造方法の変更に関する効率化のもう1つの目玉施策である年次報告の試行的導入となります。
この通知の発出をもって、製造方法等の年次報告制度を試行的に始めることとなりましたので、通知のポイントを整理しておきます。試行的かつ任意の仕組みとなりますので、これまで通り、年次報告を活用せずに軽微変更届出での変更対応も可能です。
ただし、2025年2月12日に国会提出された薬機法改正法案において、この年次報告制度(及び中等度変更制度)の内容が入ってきています。したがって、法案成立、施行となった際には本格的な制度の導入に至ることになります。薬機法改正法案については、こちらで概要を示していますが、この通知をベースにした制度となりそうです。
年次報告通知のポイント
ここからは通知の解説になります。
まず、年次報告の対象については以下が例示として挙げられています。
- 承認申請書の「製造方法欄」のうち、既に軽微変更届出事項として承認書に記載している一部のパラメータ
- 「規格及び試験方法」(別紙規格を含む。)や「成分及び分量又は本質」のテキスト欄
- 表示・保管のみを行う製造所の追加のうち現在軽微変更届出で行っているもの
- 外部試験検査機関の追加のうち現在軽微変更届出
すなわち、軽微変更届出事項のうちの一部が年次報告の対象となりうるということになります。実際に年次報告の対象となるかどうかは、個別にPMDAが審査又は相談の中で判断していくとのこと。
次に、年次報告とする事項については、承認申請書ではなく、附属文書に記載する必要があります。この対応により、年次報告事項は、承認事項ではない、という整理にしています。具体的な記載事例は、今回発出の通知の別表としてて添付されています。
また、年次報告を導入しようとする場合、事前に(承認申請前に)PMDAに相談することが求められています。この相談は、事前面談とされていますので、無料かつ常時相談申し込みが可能となります。年次報告導入に関する承認審査は優先審査として扱われるようです。
一方で、年次報告の内容については、年1回「医薬品軽微変更届事前確認相談」に申し込みPMDAの確認を受けることとされています。こちらは有料[319,900円(2025年2月時点)]の相談となります(PMDAのホームページより)。この有料でのPMDAの確認は、医薬品医療機器制度部会のとりまとめや薬機法改正法案でも触れられていた内容にはなります。ただし、実際の相談プロセスは、通常のものとは異なるとのことで、別途事務連絡が発出される旨も今回の通知で言及されています。
その他、変更がなかった場合でもその旨の年次報告が必要であること、中等度変更事項の導入と併せて対応することが可能であること、試行的実施の実施結果を確認するためPMDAから変更の製造管理の実施状況を問い合わせる可能性があること、といった点が通知で触れられています。


コメント