2024年4月18日の令和6年度第1回厚生科学審議会医薬品医療機器制度部会から、次期薬機法改正の議論が開始されています(関連記事)。
2024年11月28日に令和6年度第9回会議が開催となりました。今回は、厚労省医政局主導で議論されてきた安定供給確保について、薬機法での手当を行おうとする論点が提示されました。
また、これまでの議論のとりまとめに向けた骨子案が示されました。
安定供給確保
関連資料はこちらにありますが、資料作成責任者は(これまでの医薬局と違って)医政局となっています。そして、以下のように別会議でまとめられてきた内容になっています。

これらの内容について、結局、新規法律の制定や他の法律を模索するのではなく、薬機法下で規定していくという厚労省側の思惑が今回の会議で示されたことになります。
具体的には、総括製造販売責任者(総責)、品質保証責任者(品責)、安全管理責任者(安責)のように、「安定供給体制管理責任者(仮称)」の設置が薬機法上規定/義務化されることになります。
そして、「安定供給体制確保のための手順書(仮称)」の作成、体制整備は、薬機法18条(医薬品、医薬部外品及び化粧品の製造販売業者等の遵守事項等)に関連付けて規定されるとのこと。
そして、当該規定の順守状況の確認は、都道府県による実施が想定されています。
厚労省医政局の資料にもありますが、安定供給確保のためには多部門の関与があります。したがって、製造販売業者の中でどの部門がその主たる責任を担うのかは、各社議論になってきそうです。
とりまとめ骨子案
とりまとめ骨子案が示されました。現時点では、これまで議論されてきた項目の羅列にとどまっています。今後、来年通常国会での薬機法改正法案の提出に向けて、年内でのとりまとめに向けて実際の内容が記載されていくことになろうかと考えます。
章立てが、これまでの議論の順や、議論により時間を割いた順ではなく、
- 医薬品等の品質確保及び安全対策の強化について
- 品質の確保された医療用医薬品の供給について
- ドラッグ・ラグやドラッグ・ロス解消に向けた創薬環境・規制環境の整備について
- 医薬品へのアクセスの向上及び医薬品の適正使用の推進について
となっているあたりは配慮が感じられます。
その他、「医薬品の臨床試験の実施の基準に関する見直し」といった薬機法レベルでの改正ではなく、これまでの本会議でそれほど議論されていなかったであろう内容も入ってきています。このようなトピックについて、どのような記載がされるかは注視が必要です。
その他
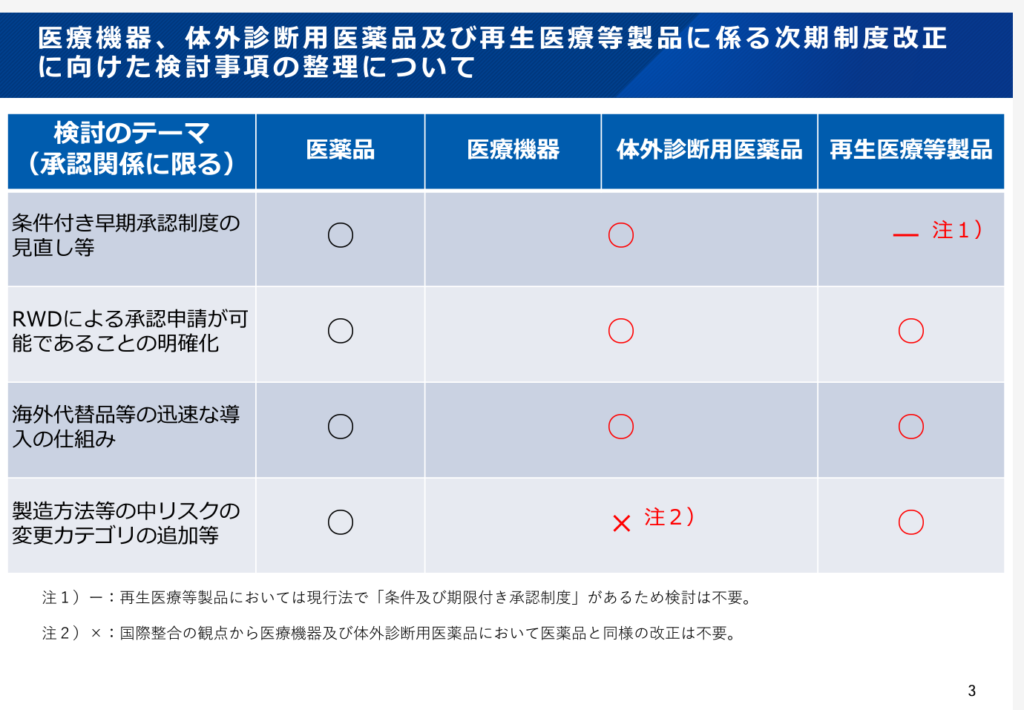
医薬品をメインに議論されたきた薬機法改正トピックについて、以下のように、医療機器、体外診断用医薬品及び再生医療等製品でも同様の改正が想定されているのかを整理したものが提示されていましたので、備忘録として残しておきます(実際の資料はこちら)。
関連リンク
- 医薬品医療機器制度部会のページ:https://www.mhlw.go.jp/stf/shingi/shingi-kousei_430263.html
- 令和6年度第9回医薬品医療機器制度部会のページ(各種資料あり):https://www.mhlw.go.jp/stf/newpage_46170.html
- 2025年薬機法改正に向けた議論の開始:https://regulatory-j.com/act-revision-2024-1/


コメント