2025年7月24日にPMDAが「新規モダリティ医薬品等薬事開発支援プログラム」の開始を公表しました(PMDAのニュースリリース)。
このプログラムは、従来の医薬品開発とは異なる技術やアプローチを用いた新規モダリティ(核酸医薬、細胞治療、遺伝子治療など)に対応してPMDAが支援するもので、アカデミアやスタートアップによる創薬イノベーションを促進することを目的としています。
ここでは、このプログラムの情報をまとめておきます。
プログラムの目的と背景
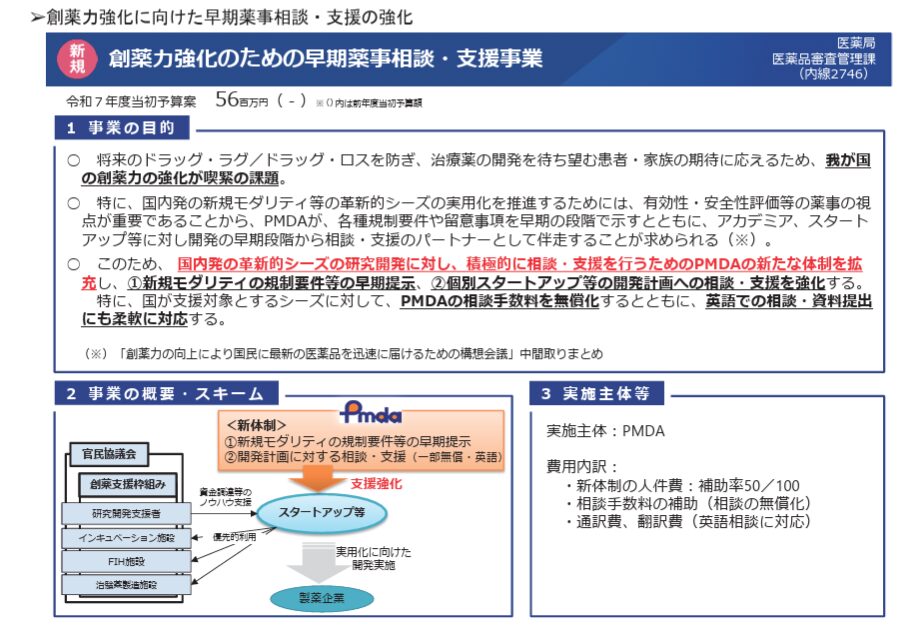
ドラッグロス対応、創薬強化に関する2024年の議論(例:創薬力の向上により国民に最新の医薬品を迅速に届けるための構想会議の中間とりまとめ、骨太方針2024)を踏まえて、2025年度用に厚労省から予算要求された以下の「創薬力強化のための早期薬事相談・支援事業」に基づき、実施されることとなったプログラムになります。
支援の対象と内容
本プログラムの対象は、国(AMEDなど)が支援する新規モダリティの医薬品等を開発するアカデミアや国内スタートアップ等です。すなわち、厚労省等の政府やAMEDの予算を使っている研究に対してのみ、本プログラムの活用の可能性があります。
支援内容は以下の通りです:
- 薬事開発上の課題の明確化:品質、薬理、薬物動態、毒性などの観点から、開発に必要な要件や留意点を提示。
- 開発計画への助言:First In Human試験(第I相試験)実施までに必要な薬事対応を中心に、複数回の面談を通じて継続的に支援。
- 専門チームによる伴走支援:PMDA内の各分野の専門家がチームを組み、開発者と対話を重ねながら課題解決を図る。

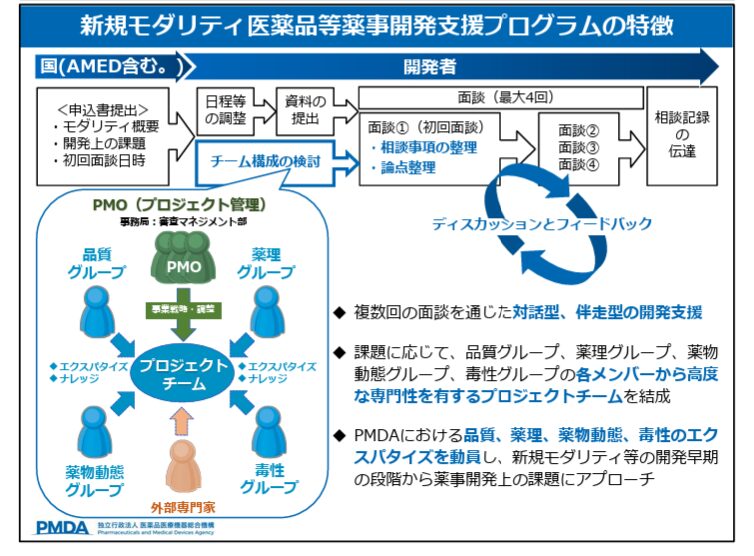
プログラムの特徴
- 部門横断型チーム編成:品質、薬理、薬物動態、毒性の各分野から専門家を集め、開発者と最大4回の面談を実施。
- 対話型・伴走型支援:単発の相談ではなく、継続的なディスカッションとフィードバック。
- 薬事規制の早期対応:新規技術に対する薬事要件を早期に明確化し、ドラッグ・ロスやドラッグ・ラグの防止を目指す。
所感
2025年度予算が2024年末に成立し、4月から執行されたことを踏まえると、本プログラムの開始が同年7月となった背景には、PMDAによる体制整備や支援内容(具体的な相談の仕組み)に関して、一定の時間と試行錯誤が必要だったことが推察されます。開始までの数か月間に、関係者間での調整や方針検討が行われた可能性もあるでしょう。
また、本プログラムは厚生労働省の予算に基づいて実施されているため、PMDAがこの取り組みをどこまで継続するのかについては現時点では不透明です。2025年度限りの事業なのか、今後も継続して展開されるのかは、政策的な方針や厚労省の予算の確保状況次第と考えられます。
さらに、厚生労働省の2025年度予算要求の概要とPMDAによる発表資料を比較すると、明確な言及がなされていない要素もいくつか存在します。ひとつは、相談支援にかかる手数料についてです。厚労省側の想定では、事業予算を活用し、相談手数料の一部を無償化する可能性が示されていました。しかしPMDAの資料ではこれに関する記述は見られません。支援対象がAMED等の研究費を得ている限られた者に絞られているため、詳細な記載を不要と判断した可能性もありますが、実際の運用方針には注目が集まるところです。
もう一つの論点は、英語による資料提出や相談の対応可否についてです。厚労省は海外スタートアップ等による本プログラムの活用も視野に入れ、英語での対応を含めていたようですが、PMDAのプログラム資料ではこの点が明示されていません。PMDAの業務量全体に与える影響を踏まえると、英語対応の範囲や優先度をどのように捉えているのかは、実務的に非常に重要な視点です。
加えて、「伴走」というキーワードは厚労省、PMDA双方が掲げていますが、PMDA資料では最大4回の相談という回数制限が記載されています。インフォーマルなコミュニケーションが別途図られる可能性はあるにせよ、支援の密度や柔軟性にどのような影響を及ぼすかについては注視する必要があります。
最後に、「対話型」の支援を謳うPMDAのアプローチは、新規モダリティ開発に対する薬事的要件の明確化を進めるという点で歓迎される一方、注意すべきリスクも存在します。すなわち、PMDAからの提示があまりに厳格または非現実的であった場合、開発者の創造的な取り組みに制約を与えてしまう恐れもあります。また、規制要件やPMDAの期待値に対し、開発者がどのように対応・工夫すべきかといった「助言」までPMDAが踏み込めるかどうかは、プログラムの有用性を左右する重要な要素と考えられます。


コメント