2024年6月3日、小児用医薬品開発計画確認相談、希少疾病用医薬品優先審査品目該当性相談、医薬品申請データパッケージ相談が新設された旨がPMDAのホームページに掲載されました。
こちらは、2023年5月~2024年3月に開催された「創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会」で示された対応方針を受けたものになります。
この検討会を受けて、ドラッグ・ロス、ドラッグ・ラグの解消等を目指して「希少疾病用医薬品等の指定制度の改正」と「小児用医薬品開発の追加インセンティブ」が導入されました。
そして、2024年5月26日付けで令和6年度「小児・希少疾病用医薬品等薬事相談センター事業」を介して、小児用医薬品開発計画確認相談、希少疾病用医薬品優先審査品目該当性相談、医薬品申請データパッケージ相談の手数料に対する助成する旨が通知されました(こちらの記事より)。
この通知発出時点で、そもそもこれらの相談の詳細が示されていませんでしたので、今回、この相談の詳細が設定されたことになります。
いずれの相談も2024年7月1日から実施依頼書の受付開始となります。
ここでは、これらの相談のポイントをまとめておきます。
小児用医薬品開発計画確認相談
PMDAのホームページは以下です。
https://www.pmda.go.jp/review-services/f2f-pre/consultations/0118.html
手数料は、1,541,600円です。助成があった場合は0円になります。
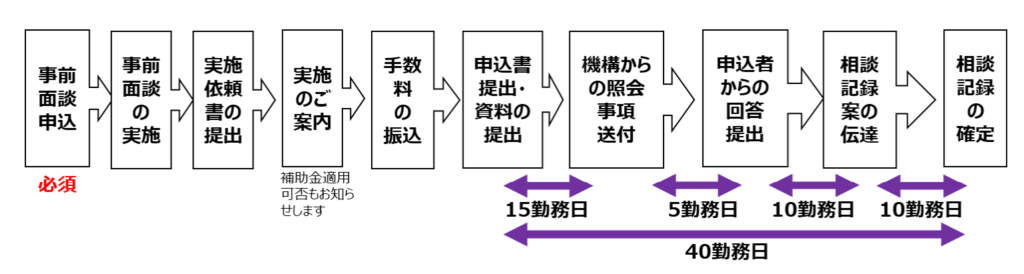
上記が相談の流れになりますが、事前面談(無料、相談のための内容整理)が必須となっています。
事前面談後、実施依頼書を提出すると、助成の対象となるかの連絡が速やかに届くことになっています。
そして、相談用の資料提出から30営業日でPMDAからの記録伝達、その後10営業日で記録の確定となります。したがって、資料提出から2か月程度で結論が確定するイメージです。
事前面談、実施依頼書の提出とも(7月1日以降)随時受け付けられることになります。
希少疾病用医薬品優先審査品目該当性相談
PMDAのホームページは以下です。
https://www.pmda.go.jp/review-services/f2f-pre/consultations/0009.html
手数料は、1,300,600円です。医薬品申請前相談ありの場合、266,400円となります。助成があった場合は半額の650,300円、133,200円になります。

上記が相談の流れになりますが、事前面談(無料、相談のための内容整理)が必須となっています。
事前面談後、実施依頼書を提出すると、助成の対象となるかの連絡が速やかに届くことになっています。
そして、相談用の資料提出から40営業日でPMDAによる評価報告書の確定となります(例示なので、期間は前後しそうです)。したがって、資料提出から2か月程度で結論が確定するイメージです。
事前面談、実施依頼書の提出とも(7月1日以降)随時受け付けられることになります。
医薬品申請データパッケージ相談
PMDAのホームページは以下です。「治験相談等(新医薬品)」のうち、16、17番に医薬品申請データパッケージ相談があります(未承認薬検討会の場合、医師主導治験の場合)。
https://www.pmda.go.jp/review-services/f2f-pre/consultations/0007.html
手数料は、7,134,300円です。助成があった場合は半額の3,567,150円になります。
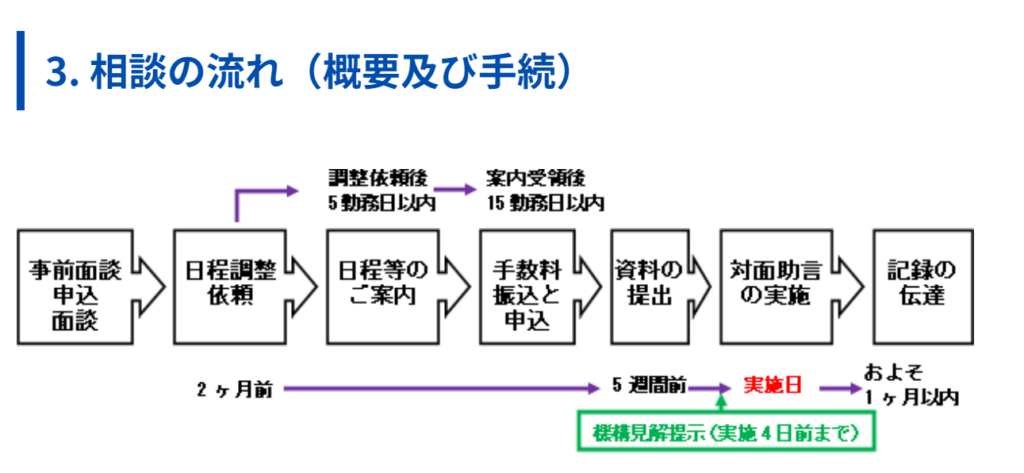
上記が相談の流れになりますが、この相談の場合は、通常の治験相談等の対面助言と同じ流れになります。


コメント